重要新闻
一管血筛两癌!北京胸科医院科研团队领衔研发“SPOGIT”模型,提升胃肠早癌及癌前病变检出率
近日,首都医科大学附属北京胸科医院消化内科何玉琦、林舒晔团队,联合中国人民解放军总医院第七医学中心盛剑秋、金鹏团队,及福建省龙岩市第一医院与山东东营市人民医院,在国际期刊 《Journal of Advanced Research》 (中科院一区,IF:13.0)上发表了题为《Clinical validation of a multi-model blood cfDNA methylation assay for early-stage gastrointestinal cancer screening》的研究论文。该研究成功开发并验证了一种基于血液cfDNA甲基化和多算法模型的新型检测技术——SPOGIT。研究证实,SPOGIT不仅能高效、准确地筛查出早期胃肠道癌症,更在癌前病变的检测上展现了重大突破。这一“筛防一体”的双模型架构(SPOGIT/CSO)有望重塑胃肠癌管理策略,显著提高患者生存率。
本研究共同第一作者为消化内科博士研究生朱玲琴、副研究员林舒晔和中国人民解放军总医院第七医学中心博士许俊锋,通讯作者为何玉琦、金鹏、郭妮和兰世迁。

研究背景与意义
胃肠道(GI)癌症是全球癌症相关死亡的第二大原因,其高死亡率主要归咎于晚期发现。尽管内镜检查是金标准,但其侵入性、资源依赖性限制了人群筛查中的广泛应用。现有的基于血清的非侵入性标志物(如CEA、CA19-9)对早期病变和癌前病变的敏感性不足,临床上迫切需要一种依从性好、非侵入、高敏感性的早期检测方法。本研究开发了一种专门针对早期胃肠癌及癌前病变的优化的血液检测方法,或可满足大规模人群筛查的需求。
创新性亮点
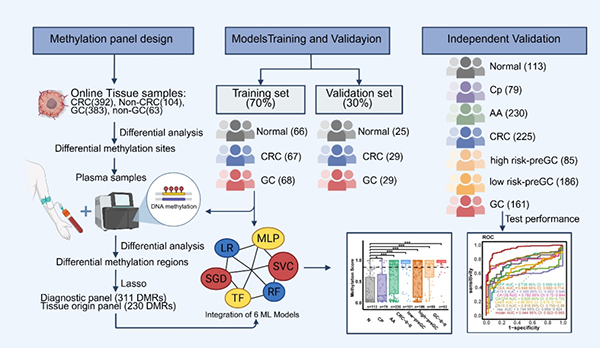
研究团队通过对海量甲基化数据进行深度挖掘,并结合多种机器学习算法 ,构建了SPOGIT(胃肠道肿瘤筛查)模型和CSO(癌症信号起源)模型。在一个包含1079例样本的大型多中心独立验证队列中 ,SPOGIT展现了卓越的性能:
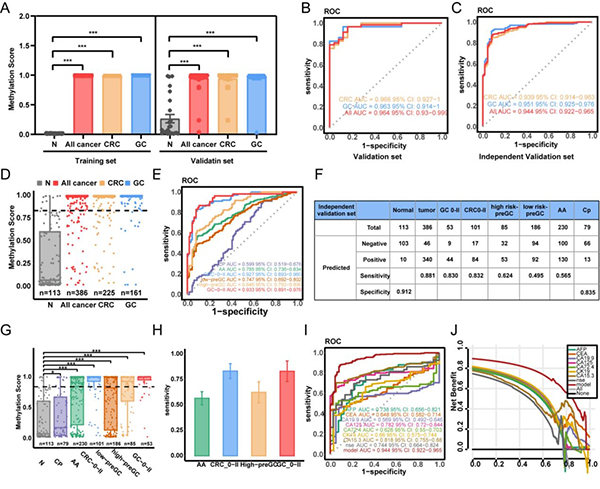
1. 高准确性: SPOGIT在大型验证集中的整体表现强劲,对胃肠道癌症检测的敏感性达到88.1%,特异性达到91.2%。
2. 强大早癌检出能力: 该模型对早期(0-II期)癌症的检测敏感性高达83.1% ,远优于传统血清标志物。
3. 突破性癌前病变拦截:SPOGIT能够有效“拦截”癌前进展,对晚期腺瘤的检出敏感性为56.5%,对高风险胃癌癌前病变的敏感性达62.4%。
4. 精准肿瘤溯源: 配套的CSO(癌症信号起源)模型能有效区分癌症器官来源,对结直肠癌的溯源准确率为83%,对胃癌的准确率为71% ,可指导阳性患者进行下一步的结肠镜或胃镜检查。
5. 便捷可及:该检测仅需10毫升外周血,且对cfDNA输入量要求低(<30 ng),非常适合在资源有限的环境和大规模人群中推广。
临床价值与展望
SPOGIT/CSO双模型架构的临床应用价值较高,研究团队通过拦截模型进行模拟分析,结果显示: SPOGIT的应用预计可使晚期(III/IV期)胃肠癌的诊断比例降低92%,通过早期发现和干预,预计可将胃肠癌患者的5年生存率提高27.02%至30.47%。
本研究提出的临床工作流程清晰地展示了其应用前景:筛查人群(推荐40-75岁)接受SPOGIT血液检测 ;阴性者返回常规筛查 ;阳性者则启动CSO模型分析,根据其胃癌或结直肠癌的预测信号,精准指导患者进行后续的胃镜或结肠镜检查。这项研究提供了一种高准确性、微创便捷的胃肠道癌症和癌前病变筛查新策略。SPOGIT/CSO模型作为一种方便快捷的筛查工具,有望通过早期拦截显著降低胃肠癌的发病率和死亡率,为全球公共卫生带来巨大益处。







.jpg)

















